Toute la matière qui vous constitue, qui constitue ce délicieux morceaux de chocolat vraiment trop tentant, qui constitue votre maison, vos amis, vos ennemis, vos animaux de compagnie, la Terre et les autres planètes, le Soleil et les autres étoiles jusqu’aux limites de l’univers observable… n’est qu’un grand Lego construit avec 94 types de brique différents, appelés « éléments chimiques ». Encore mieux, toutes ces briques ne sont en fait composés que de trois types de particules : protons, neutrons et électrons. Mais n’allons pas trop vite, et prenons nos pinceaux…
Esquisse d’un tableau
Même si nous ne retracerons pas ici cette histoire, sachez que, depuis la nuit des temps, l’homme fait de la chimie sans le savoir, et cela dès qu’il a mélangé ou fait cuire différents types de matière pour obtenir… d’autres types de matière.
L’homme s’est ainsi rendu compte qu’un type de matière pouvait être fait de plusieurs types de matière, tel le bronze qui est un mélange de cuivre et d’étain. La question s’est alors posée de savoir si certains types de matière pouvaient, eux, ne pas être décomposable, ce que l’on appelle aujourd’hui les éléments chimiques. L’eau a, par exemple, perdu ce titre en 1800 lorsqu’on a su la décomposer en hydrogène et oxygène, par électrolyse (c’est à dire à l’aide d’un courant électrique, une expérience qu’il n’est pas très utile de tenter dans votre bain).
Au cours du 19ème siècle, on cherchera à établir cette liste d’éléments chimiques. Et c’est là, en 1869, qu’intervient notre ami Dmitri Mendeleïev (photo ci-dessous). Ce chimiste russe remarqua qu’en classant tous les éléments alors connus par ordre de masse, un certain cycle semblait se répéter quant à leurs propriétés chimiques.
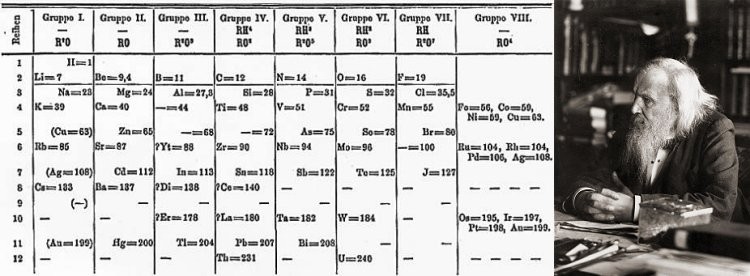
Il eut l’idée de les placer dans un tableau, toujours par ordre de masse, de gauche à droite et de haut en bas, en regroupant dans une même colonne les éléments possédant à peu près les mêmes propriétés chimiques. Et cela fonctionnait bien : aucun de ces éléments ne perturbait le bel édifice en venant s’intercaler là où il ne fallait pas. Le rangement par masses faisait bien apparaître un cycle lié aux propriétés chimiques de ces éléments.
Pour dire vrai, il y avait tout de même un gros problème avec ce classement périodique des éléments : plusieurs cases de son tableau étaient… vides. En effet, à quelques reprises, pour respecter son principe de classement, il avait dû, d’un élément à un autre, sauter une ou plusieurs colonnes.
Alors, tout faux le Dmitri ? A la poubelle le classement périodique des éléments ? Pas du tout, rétorqua t-il, si ces cases sont vides, c’est parce qu’il devait s’y trouver des éléments chimiques que nous ne connaissions pas encore ! Et comme c’est son tableau qui devait avoir raison, il indiqua par avance, pour chacun de ces éléments inconnus, quelles seraient ses propriétés chimiques et quelle serait approximativement sa masse (située entre celle de l’élément connu qui le précède dans le tableau, et celle de l’élément connu qui le suit).
Et vous savez quoi ? Les années passèrent, et on découvrit, l’un après l’autre, les éléments chimiques manquants. Qui plus est avec les propriétés prévues par Mendeleïev !…
Trop fort le Dmitri.
Présentation du tableau
Voici ce fameux « Tableau périodique des éléments » tel qu’il apparaît aujourd’hui. Il est assez différent de celui que Mendeleïev avait conçu à l’origine mais il repose sur le même principe.
(vous pouvez cliquer sur l’image pour l’agrandir… puis fermer l’onglet pour revenir ici).
On y retrouve les 94 éléments dont je vous parlais en introduction : les 94 briques du grand Lego universel. Du plus léger, l’hydrogène, au plus lourd, le plutonium. En fait, la plupart de ces éléments sont extrêmement rares. A lui tout seul, l’hydrogène représente 74% de la masse de l’ensemble (dans l’univers, pas sur la Terre), et l’hélium 24% ! Il ne reste que 2% pour les autres éléments… dont 1% pris par le seul oxygène. Suivent ensuite le carbone, le néon, le fer, l’azote, etc. et des chouias de chouias pour le reste.
94, pas un de plus ?
En fait, si… Il en existe encore d’autres, plus lourds, que l’on est parvenus à créer artificiellement (de plus en plus difficilement) mais leur durée de vie est – croyez-moi – ridicule. Ces grosses briques se cassent aussitôt en briques plus petites (celles du tableau). A l’heure où j’écris ces lignes, on est ainsi parvenu jusqu’à l’élément 118. Il n’est pas impossible que l’on parvienne, dans l’avenir, à créer des éléments encore plus lourds qui puissent être un peu plus stables (avec une durée de vie gigantesque de quelques minutes) mais cela reste très théorique. Au-delà d’un hypothétique élément 137 (ou 173, selon les théories), des effets relativistes (l’impossibilité pour l’électron d’aller plus vite que la lumière) mettent un terme à la course au plus lourd.
Enfin peu importe, ce sont bien ces 94 éléments qui constituent ce que vous appelez la matière.
Mais cette matière est loin d’avoir livrer tous ses secrets : allons voir maintenant ce qui se cache derrière ce tableau…
Bonus vidéo
En bonus, je vous propose de découvrir l’excellente vidéo concoctée par Bruce sur sa chaîne E-Penser au sujet de notre ami Mendeleïev et de son tableau (avec plein d’infos que je ne me suis pas embêté à écrire)…
Le joli tableau de Mendeleïev
- Partie 1 : Esquisse et présentation du tableau
- Partie 2 : Derrière le tableau
- Partie 3 : La chimie dans le tableau
- Partie 4 : Le nucléaire dans le tableau





